

在重组蛋白制备中,Yeast Expression Systems(酵母表达系统)占据着连接微生物生长速度与真核生物修饰能力的独特生态位。作为单细胞真核生物,酵母不仅拥有完整的内膜系统来进行蛋白质折叠与修饰,还能在廉价的无机盐培养基中实现极高的生物量积累。
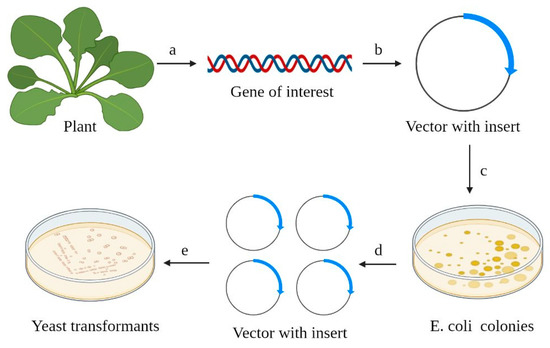
在重组蛋白制备体系中,酵母表达系统占据着连接“微生物生长效率”与“真核修饰能力”的关键位置。作为单细胞真核生物,酵母既具备内质网—高尔基体分泌通路,能够完成二硫键形成与糖基化修饰,又保留了类似细菌的高生长速率和对廉价培养基的适应能力。
从工业与结构生物学的双重视角看,毕赤酵母和酿酒酵母构成了真核蛋白生产的重要底盘。其中,毕赤酵母因其严格调控的启动子系统、整合型表达策略以及对高密度发酵的高度适配性,逐渐成为毫克级到千克级蛋白生产的主流选择。
毕赤酵母表达体系的技术核心在于 AOX1 启动子,这是目前已知调控最严格、诱导强度最高的真核启动子之一。其转录调控遵循典型的三态机制:在葡萄糖或甘油存在时完全阻遏,在碳源耗尽后进入解阻遏状态,而在甲醇存在下被强烈激活。甲醇不仅是碳源,更是转录调控信号分子。其代谢激活特异性转录因子(如 Mxr1),从而驱动 AOX1 启动子进入极晚期高转录状态。在诱导阶段,目标蛋白的表达可占细胞总可溶性蛋白的显著比例,使资源在时间维度上被高度集中到产物合成。
这一“代谢—转录耦合”的设计,使细胞生长与蛋白表达在时间上严格分离:前期最大化生物量积累,后期集中进行蛋白生产,从根本上降低了毒性蛋白对宿主生长的干扰。
酵母系统在下游纯化中的突出优势,来源于其高效的分泌表达能力。通过融合来源于酿酒酵母的 α-交配因子信号肽,新生肽链被导入内质网腔,进入经典分泌途径。在高尔基体中,Kex2 蛋白酶识别并切割特定的碱性二肽位点,而 Ste13 进一步去除残余的前导序列,最终释放具有天然 N 端的成熟蛋白。这一分级加工机制在正常表达负荷下具有极高的准确性。
然而,在超高表达条件下,分泌加工系统可能成为限速步骤。Kex2 或 Ste13 的酶学容量不足,会导致信号肽残留或 N 端异质性。通过共表达加工蛋白、优化信号肽结构或降低单位时间合成速率,是维持分泌质量的常规工程手段。
作为真核系统,酵母能够进行 N-糖基化修饰,但野生型菌株以高甘露糖型糖链为主,其结构与人体存在显著差异。在药用蛋白生产中,这种差异可能引发免疫原性或快速清除问题。通过糖基化工程,研究人员可敲除关键甘露糖转移酶,并引入外源糖链修饰酶,从而构建人源化糖基化路径。经过改造的毕赤酵母能够合成结构更接近哺乳动物细胞的复杂型糖链,使其在某些生物药领域具备实际可行性。
在工艺层面,酵母系统的另一核心优势在于高密度发酵能力。通过精确控制溶解氧、补料速率与甲醇负荷,可将细胞维持在“代谢受限但表达活跃”的状态,使体积产率达到极高水平。这种工程与代谢协同优化,使酵母成为成本效益极高的工业表达平台。
总体而言,酵母表达系统通过强诱导启动子实现高表达,通过分泌通路降低纯化复杂度,并通过糖基化工程不断逼近高端应用需求。其真正价值不在于替代哺乳动物细胞,而在于在表达效率、成本控制与修饰能力之间建立高度工程化的平衡。对于大量结构蛋白、酶类及部分治疗性蛋白而言,酵母依然是当前最具工业竞争力的真核表达底盘之一。